
シリーズ 先端医療 ―樹状細胞療法― ③
進行がん・転移がんの最終兵器
悪性因子TGF‐βを狙う分子樹状細胞療法
―バイオ薬品化する免疫細胞の威力
星野泰三
東京・京都統合医療ビレッジグループ理事長 プルミエールクリニック院長
進行がん・転移がんの治療は、通常の標準治療を行っても、免疫細胞療法を駆使しても困難であるのは間違いありません。その大きな要因の1つが、がんというものが進行・転移してしまう性質を持ち合わせていることです。
がんが進行・転移する理由の1つに「TGF–β(ベータ型トランスフォーミング増殖因子)」が深く関わってきていることが解明されてきました。そして、このTGF–βの対策として、バイオ薬品化された分子樹状細胞がその切り札として注目を集めています。
そこで、本連載の3回目は、悪性因子TGF–β対策としての分子樹状細胞療法を取り上げました。
進行・転移の原因が解明
TGF–βは、免疫細胞を含めて多くの細胞の増殖を抑制します。また、進行・転移したがん細胞から、あるいはその周囲の間質の組織からつくり出されます。そして、活性化したTGF–βは、がんの血管新生や免疫力低下といった悪い作用をもたらします。その結果、がん細胞の運動能が高まったり、がんの浸潤の誘導・転移が促進されたりしてしまうのです。
このように、がんの進行と正比例の関係にあるTGF–βは、ある意味で生物学的な腫瘍マーカーとも言われています。ですから、当院においても免疫解析(抗がん細胞活性・良い免疫ホルモン・悪い免疫ホルモン・がんの血管新生因子を調べる検査)をして、患者さんのTGF–βの状態を把握することに注力しています。
TGF–βは、がん細胞のEMT(epithelial mesenchymal transition)を誘導し、がん細胞の運動や浸潤を亢進させる作用があります。EMTとは上皮間葉転換のことで、がんの浸潤や転移を誘導する〝くせ者〟で、例えるならがん細胞が城を築くうえで重要な〝支持母体〟をつくってしまう存在なのです。
それと同時に、TGF–βには、がんの周囲の間質に対し、血管新生や細胞外マトリックス(生物において、細胞の外に存在する超分子構造体)産生、免疫抑制などの作用があります。このような状況になってしまうと、その部分にリンパ球が近寄れなくなり、よりがんを進行させてしまうのです。したがって、がんの進行に重要な働きをするTGF–βを抑える免疫細胞療法が開発されれば、副作用の少ない〝抗がん剤〟となり得るはずです。
具体的な「TGF–βによるがん転移促進の機序」には、HMGA2タンパク質などさまざまな転写因子が重要な働きを担っているなどの解明が進んできました。そして、昨今の研究では、TGF–βによるEMTは、乳がん細胞のがん幹細胞マーカーの発現を促したり、がん細胞の運動・浸潤能の亢進だけでなく自己複製能や腫瘍形成能の亢進も促進したりすることがわかってきました。
がん幹細胞は言うなればがんの〝女王蜂〟ですから、転移した先々でもがんが自ら増え続ける仕組みをTGF–βがどんどんつくってしまっている、ということが言えます。
また、TGF–βは、がん細胞以外に、がんの周囲にある間質に対しても大きな作用を持っています。その働きとしてまず挙げられるのは、がんの周囲に存在するCAF(Cancer associated fibrob-last)と呼ばれる線維芽細胞や筋線維芽細胞との関連性です。この2つの細胞はがんの増殖・浸潤・転移において重要な働きを持っていて、TGF–βは間葉系前駆細胞からの線維芽細胞や筋線維芽細胞への分化を誘導してしまうのです。
そして、TGF–βは、アバスチンなどのモノクローナル抗体でも知られるVEGF(血管内皮細胞増殖因子)などの発現を誘導し、腫瘍の血管新生を亢進させる働きも持っています。さらに、先述した浸潤に加え、遠隔転移の多段階において、さまざまなメカニズムを介して転移を促進させていることもわかっています。ちなみに、がんの転移は、局所での浸潤、血管内への侵入、血中での生存、遠隔臓器での血管外遊出、その臓器での生着・増殖といった多段階のステップにより成り立っています。
その他のTGF–βの負の特徴は、細胞溶解に働く因子の発現抑制により、キラーT細胞の活性を阻害し、抗原提示細胞によるT細胞の活性化を抑制し、さらにヘルパー細胞やNK細胞、マクロファージなどに対しても抑制的に働いて、がんに対する生存の防御機構を崩してしまうことです。こうしたTGF–βの作用によって、免疫細胞療法は効きにくくなっているのです。
このようなTGF–βに関する研究では、たとえば乳がん細胞株を用いたものでは「TGF–βのシグナルを阻害すると、肺転移や肝転移が抑制された」という結果も出ています。それに対し、TGF–βはがん細胞が転移した臓器において産生されますので、乳がん・前立腺がんといった比較的、骨転移が多いがんでは、転移した骨の中でTGF–βがつくられるということもわかっています。そうなると、TGF–βによって、がん細胞から産生される因子が骨破壊を促進し、それにより骨基質からTGF–βの放出が亢進するという悪循環に陥ってしまいます。
そのような負のスパイラルを絶つ治療法として、分子樹状細胞療法が耳目を集めているのです。
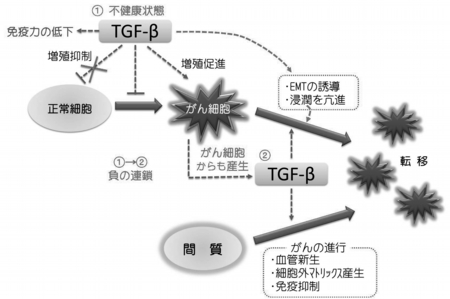
図1 体内環境の悪化など不健康状態では、TGF-βが産生され、免疫力の低下、がんの増殖・転移を招き、さらにがん細胞自体からも2次的にTGF-βを産生するという負のスパイラルを引き起こす。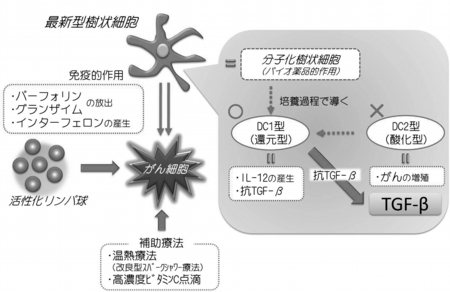
図2 負のスパイラルを食い止めるためにも、分子化樹状細胞をバイオ薬品的に使用することが期待される。
分子樹状細胞で、悪循環を断つ
樹状細胞は、標的となるがん細胞に接着し、その抗原提示能力により、キラーT細胞を強力に誘導する作用を持っています。その働きによって、パーフォリンやグランザイムという抗がん酵素が放出されやすくなる、インターフェロンが産出されやすくなる、といった免疫的作用が期待できるようになるのです。
TGF–βを標的誘導した分子樹状細胞にはTGF–βの働きを抑える作用があることがわかってきたのですが、それがまさしく「バイオ薬品化する免疫細胞の威力」、すなわち分子樹状細胞療法ということになります。
分子樹状細胞によるTGF–β対策の大きなポイントは、DC1型(還元型)の樹状細胞を用いるということです。というのも、樹状細胞には、DC1型とDC2型(酸化型)という2つのタイプが存在します。
前者は、IL(インターロイキン)–12というサイトカインを産生し、腫瘍塊の中にキラーリンパ球を誘導して免疫治療の効率化を図ります。それに対し、後者はTGF–βをはじめ、悪液質の元となるカケクチンなどを誘導させてがんの増殖能を高めてしまうこともありますし、がんを他の部位に誘導して転移を引き起こす腫瘍誘導という恐ろしい作用も持っています。
したがって、培養技術によって、樹状細胞をDC2型からDC1型に導くことが、1つのTGF–β対策となるのです。ですから、DC1型となった樹状細胞を患者さんの体内に戻す分子樹状細胞療法を行うとき、必要であればTGF–βを抑えるような活性化を持たせなければなりません。
また、患者さんの病巣が血流の悪い低酸素状態になると、腫瘍組織細胞をはじめとする各種浸潤細胞によってTGF–βをはじめIL–10、VEGF、PGE2などの悪性の物質が産生され、逆に樹状細胞内のグルタチオンの産生が低下し、よりDC2型に招きやすい状態になっていきます。
そこで当院では、分子樹状細胞療法の補助療法として、局所温熱療法の1つである改良型スパークシャワー療法や、超高濃度ビタミンC点滴療法を行っています。そうすることで、樹状細胞からサイトカインが出て、樹状細胞の数も活性度も増強されるのです。
逆に言えば、このような活性化させた分子樹状細胞療法を行うことで、IL–12の産生が上昇してCD2型がCD1型化するのです。したがって、いかにTGF–βによる腫瘍組織および腫瘍周囲での悪循環を絶つのか、ということが進行性・転移性のがん治療の要諦になるのです。
しっかり調べて、しっかり治す
先述のように、当院では免疫解析を行い、患者さんの免疫状態をしっかり調べてから治療に臨んでいます。この「しっかり調べる」ということが「しっかり治す」ということにつながるはずです。
今回、ご紹介している「TGF–β対策」に関して言えば、その患者さんに最適の分子樹状細胞を培養し、場合によっては最善の補助療法を併用しています。その1例を挙げると、当院では次のようなケースがありました。
その患者さんは、免疫力を高め、心身のバランスをとることに留意されている自然療法家でした。この方が乳がんを発症させたのは今から約5年半前のこと。そのときは地元の病院で乳房温存術を受け、4~5年間は転移・再発もなく過ごしていたようです。しかし、2010年初冬に空咳が続くようになり、地元の病院で診察・検査を受けたところ再発と肺の左上葉への転移が認められました。
再発・転移に加え、この患者さんの乳がんは、トリプルネガティブ(エストロゲン受容体・ヒト表皮細胞成長因子2・プロゲステロン受容体のすべてが陰性のタイプ)に近く、主治医から抗がん剤の使用を勧められました。それでも、副作用を恐れて抗がん剤の使用を拒否。化学療法以外の治療法への可能性を求め、当院を受診したというわけです。
この患者さんが、初めて当院にいらしたときは、激しく咳き込んでおり、うつ傾向にあったようです。また、この患者さんは「楽しみながらがんを治したいので、体に悪い治療は受けたくない」といった、病状からかけ離れた治療法を希望されていました。
当院では、この患者さんの治療に対する要望を可能な限り受け入れ、かつ効果的な治療法を実施することにしました。そこで、提示したプロトコールは、活性化させた分子樹状細胞療法と自己活性化リンパ球療法の併用を2カ月間にわたり行うというものです。 分子樹状細胞療法の活性化は、患者さんの血液から採取した樹状細胞の元を免疫活性物質や人工抗原免疫賦活剤などを用いて改良・増強させて行います。もちろん、先述のように、ここでのポイントは、「還元型」という抗酸化作用に優れたタイプの樹状細胞を培養して用いることです。
分子樹状細胞は自己活性化リンパ球療法の奏効率をアップさせます。ですから、活性化させた分子樹状細胞療法を行った後に、体外で活性化させたリンパ球を注入すると、がんの固有情報が樹状細胞から伝えられ、ヘルパー1型Tリンパ球の強力な誘導により、キラーT細胞から抗がん酵素が出てがんを攻撃する、というスタイルが確立されるのです。
この自己活性化リンパ球療法は、当院では患者さんから採取したリンパ球を、付属中央研究所で2週間ほどかけて約1000倍に増殖させることから始めます。そして、サイトカインを加えることで大量かつ活性化した力強いNK細胞をつくり出しています。
今回の患者さんへの活性化分子樹状細胞療法と自己活性化リンパ球療法は、週1回のペースで8回行いました。そのなかで3回目が終了した頃には、ほとんど咳が出なくなっていました。
この分子樹状細胞療法と自己活性化リンパ球療法による2カ月余りの治療が終わると、患者さんも体調の回復を自覚できたらしく、自ら希望して地元の病院で検査を受けました。すると、再発部位も転移部位も完全に消失していたことが判明したのです(写真1)。
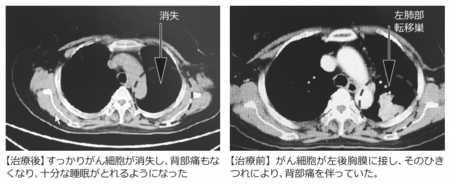
写真1
今回のようにトリプルネガティブに匹敵する乳がんに対して分子樹状細胞療法が著効したのは、患者さんのHLA(ヒト白血球型抗原)のタイプが、がん由来の物質(ペプチド)に結合しやすかったこと、多発病巣がなく骨への転移もなかったことなどがその理由に挙げられます。もちろん、治療前に免疫解析によってTGF–βをはじめとする免疫状態をよく調べたことも、寛解へと導くことができた大きな要因であるのは言うまでもありません。
(2011年10月20日発行 ライフライン21がんの先進医療vol.3より)
Life-line21 Topic
バックナンバー
 『ライフライン21 がんの先進医療』は全国書店の書籍売り場、または雑誌売り場で販売されています。以下にバックナンバーのご案内をさせていただいております。
『ライフライン21 がんの先進医療』は全国書店の書籍売り場、または雑誌売り場で販売されています。以下にバックナンバーのご案内をさせていただいております。
掲載記事紹介
 「ライフライン21 がんの先進医療」で連載されている掲載記事の一部をバックナンバーからご紹介します。
「ライフライン21 がんの先進医療」で連載されている掲載記事の一部をバックナンバーからご紹介します。
定期購読は受け付けておりません。
 「ライフライン21 がんの先進医療」は、VOL.57をもちまして終刊となりました。
「ライフライン21 がんの先進医療」は、VOL.57をもちまして終刊となりました。
全国がん患者の会一覧
 本欄には、掲載を希望された患者さんの会のみを登載しています。
本欄には、掲載を希望された患者さんの会のみを登載しています。
[創刊3周年記念号(vol.13)]掲載
がん診療連携拠点病院指定一覧表
 (出所:厚生労働省ホームページより転載)
(出所:厚生労働省ホームページより転載)
緩和ケア病棟入院料届出受理施設一覧

資料提供:日本ホスピス緩和ケア協会 http://www.hpcj.org/list/relist.html
先進医療を実施している医療機関の一覧表
 (出所:厚生労働省ホームページより「がん医療」関連に限定して転載)
(出所:厚生労働省ホームページより「がん医療」関連に限定して転載)
 詳しくはこちら
詳しくはこちら 詳しくはこちら
詳しくはこちら 詳しくはこちら
詳しくはこちら
 TOP
TOP 会社案内
会社案内 お問い合わせ
お問い合わせ ギャラリー
ギャラリー 書籍案内
書籍案内 Lifeline21 Topics
Lifeline21 Topics